
試驗信息
試驗分期:Ⅰ期、Ⅱ期、Ⅲ期
藥品名稱:SHR-A1811
適應癥:經治復發/轉移宮頸癌、卵巢癌、子宮內膜癌
患者畫像:HER2 表達的婦科惡性腫瘤患者(包括復發性卵巢癌、子宮內膜癌、宮頸癌患者)
試驗專業題目
評價注射用SHR-A1811治療HER2表達晚期宮頸癌、復發性卵巢癌及子宮內膜癌的有效性、安全性。
主要入選標準
1、18~75 周歲,ECOG 評分:0~1 分,預期生存期≥12 周;
2、研究分別入組晚期宮頸癌、復發性卵巢癌及子宮內膜癌患者:
隊列 1 復發性卵巢癌:
組織病理學確診的復發性卵巢上皮癌、輸卵管癌或原發性腹膜癌,既往經過以鉑類為基礎的方案治療,且最后一次含鉑治療方案治療期間或治療結束(完成 4 程及以上治療)后<6 個月進展或復發;針對鉑耐藥/鉑難治復發性卵巢癌,接受過不超過 1 個非鉑方案治療。
注:復發或進展的定義(滿足以下任一條件):a)有明確記錄的影像學進展;b)CA-125 持續升高。
隊列 2 子宮內膜癌:
組織病理學確診的子宮內膜癌(除外癌肉瘤),經過初始治療后出現復發/轉移的患者;既往針對復發/轉移階段經過至少 1 線、且不超過 2 線系統治療(除外放療增敏的化療),治療期間或治療結束后出現疾病復發或進展。
隊列 3 宮頸癌:
組織或細胞學證實的宮頸癌;既往針對復發/轉移性宮頸癌經過至少 1 線、且不超過 2 線系統治療(除外放療增敏的化療),治療期間或治療結束后出現疾病復發或進展;
注:新輔助或輔助治療(除外放療增敏的化療),如在初始治療規范手術后 1 年、放療后 6個月內疾病復發、進展,計為一線系統治療。
參與機構
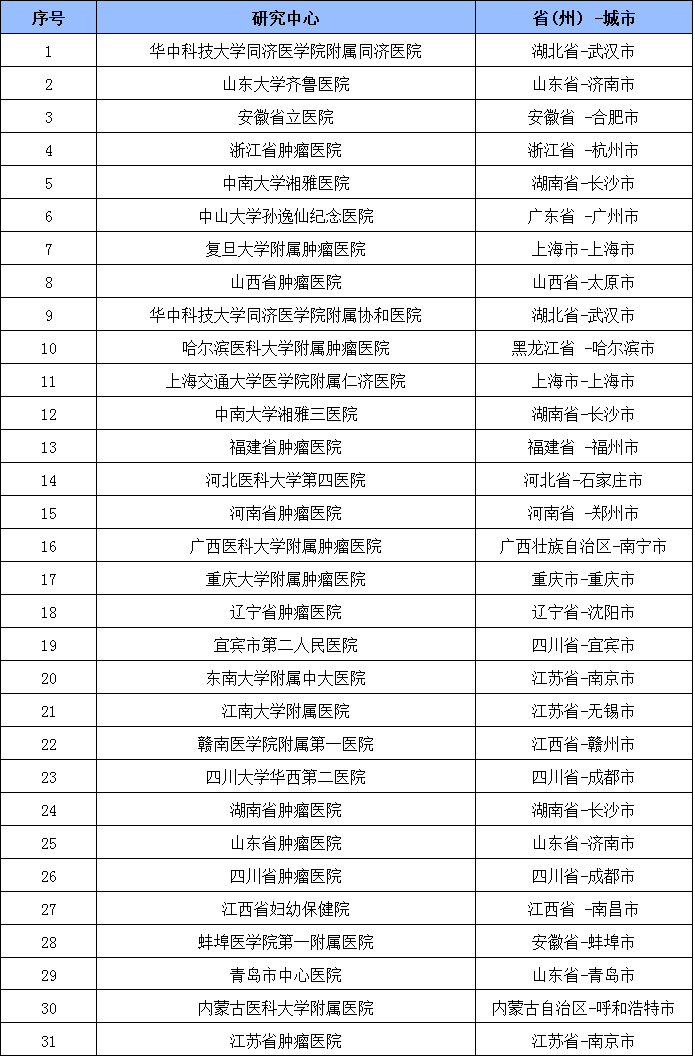
試驗信息
試驗分期:Ⅰ期、Ⅱ期、Ⅲ期
藥品名稱:SHR-A1811
適應癥:經治復發/轉移宮頸癌、卵巢癌、子宮內膜癌
患者畫像:HER2 表達的婦科惡性腫瘤患者(包括復發性卵巢癌、子宮內膜癌、宮頸癌患者)
試驗專業題目
評價注射用SHR-A1811治療HER2表達晚期宮頸癌、復發性卵巢癌及子宮內膜癌的有效性、安全性。
主要入選標準
1、18~75 周歲,ECOG 評分:0~1 分,預期生存期≥12 周;
2、研究分別入組晚期宮頸癌、復發性卵巢癌及子宮內膜癌患者:
隊列 1 復發性卵巢癌:
組織病理學確診的復發性卵巢上皮癌、輸卵管癌或原發性腹膜癌,既往經過以鉑類為基礎的方案治療,且最后一次含鉑治療方案治療期間或治療結束(完成 4 程及以上治療)后<6 個月進展或復發;針對鉑耐藥/鉑難治復發性卵巢癌,接受過不超過 1 個非鉑方案治療。
注:復發或進展的定義(滿足以下任一條件):a)有明確記錄的影像學進展;b)CA-125 持續升高。
隊列 2 子宮內膜癌:
組織病理學確診的子宮內膜癌(除外癌肉瘤),經過初始治療后出現復發/轉移的患者;既往針對復發/轉移階段經過至少 1 線、且不超過 2 線系統治療(除外放療增敏的化療),治療期間或治療結束后出現疾病復發或進展。
隊列 3 宮頸癌:
組織或細胞學證實的宮頸癌;既往針對復發/轉移性宮頸癌經過至少 1 線、且不超過 2 線系統治療(除外放療增敏的化療),治療期間或治療結束后出現疾病復發或進展;
注:新輔助或輔助治療(除外放療增敏的化療),如在初始治療規范手術后 1 年、放療后 6個月內疾病復發、進展,計為一線系統治療。
參與機構
