
試驗信息
試驗分期:Ⅱ期
藥品名稱:MWN101 注射液
適應癥:2型糖尿病
評價MWN101 注射液治療 2 型糖尿病的有效性、安全性及藥代動力學特征的隨機、雙盲、安慰劑及陽性藥平行對照、多中心Ⅱ期臨床研究
主要入選標準
滿足下列所有入選標準才可入選本試驗:
1.(問診)年齡在 18~75 周歲之間(含)且符合《中國 2 型糖尿病防治指南(2020 年版)》診斷標準的中國成人2型糖尿病患者,且滿足以下任意一條標準:
(1) 診斷為2型糖尿病的初治患者,已接受至少8周的飲食和運動干預,且既往未服用過抗糖尿病藥物,或者
(2) 既往診斷的2型糖尿病患者,目前處于飲食和運動干預期,篩選前 8 周內未接受糖尿病藥物治療,經研究者對其病情評價,可以在生活方式干預的基礎上增加試驗藥物治療;
2.(檢查)篩選時體重指數(BMI):23.0kg/㎡≤BMI≤40.0kg/㎡;
3.(檢查)篩選/基線時糖化血紅蛋白(HbA1c)中心實驗室檢測結果滿足:7.0%≤HbA1c≤10.5%;
4.(檢查)篩選/基線時空腹血糖(FPG):FPG≤13.3 mmol/L(如存在影響血糖的特殊因素可在 1 周內復測 1 次);
5.(問診)能夠按照方案要求完成試驗,自愿作為受試者,并簽署知情同意書。
主要排除標準
1.(問診)篩選前12個月內發生過嚴重的糖尿病急性并發癥;
2.(問診及檢查)篩選時存在嚴重的糖尿病慢性并發癥;
3.(問診)篩選前 6 個月內發生過3級低血糖;
4.(問診及檢查)篩選期前6個月發生過以下心血管疾病,如心力衰竭(NYHA 分級為 III-IV 級)、心肌梗塞、冠狀動脈旁路移植術或冠脈支架植入病史、需要治療的嚴重的心律失常,如Ⅱ度或Ⅲ度的房室傳導阻滯、長 QTC 綜合征或 QTc 間期延長(QTcF 女性≥470 ms 或男性≥450 ms);
5.(問診)篩選前 6個月患有出血性或缺血性腦卒中、短暫性腦缺血;
6.(檢查)篩選時甲狀腺功能檢查結果存在具有臨床意義的異常且需要啟動治療;
7.(檢查)篩選時經治療未控制的高血壓(收縮壓≥160 mmHg 和/或舒張壓≥100 mmHg);
8.(問診)既往有急性或慢性胰腺炎病史或臨床證據者;
9.(問診)已知屬于過敏體質(對3種及以上食物或藥物過敏),或對試驗用藥品或其他 GLP-1 受體激動劑類藥物過敏,或篩選時患有嚴重變態反應性疾病(哮喘、蕁麻疹、濕疹性皮炎等);
10.(問診)篩選前采用以下任何一種藥物治療:
(1) 篩選前1年內使用過胰島素,以下情況除外:①使用胰島素治療妊娠糖尿病,②因急性疾病、住院期間或擇期手術等而短期使用(≤2 周)胰島素;
(2) 篩選前 8 周曾使用過其他可能影響血糖代謝的藥物,如其他降糖藥物、全身性糖皮質激素(吸入性或局部外用除外)、生長激素等;
11.(檢查)篩選或基線時實驗室檢查結果符合以下標準的受試者:
(1) 空腹C肽<0.81 ng/mL(0.27 mmol/L);
(2) ALT、AST≥2.5×ULN或血總膽紅素≥1.5×ULN;
(3) 血淀粉酶或血脂肪酶≥1.5×ULN;
(4) 腎小球濾過率(eGFR)<60 mL/min/1.73m2 (CKD-EPI公式)或尿蛋白陽性 2+ 及以上;
(5) 血清降鈣素水平≥35 ng/L(pg/mL);
(6) 甘油三酯≥5.64 mmol/L(500 mg/dL;如為生活方式所致異常,則可在 1 周內復測 1 次);
(7) 血紅蛋白(HGB)<100 g/L;
(8) 乙肝表面抗原(HBsAg)陽性且乙肝病毒載量(HBV-DNA)高于當地實驗室檢測下限值;或丙肝抗體(HCV-Ab)陽性且丙肝病毒載量(HCV-RNA)高于當地實驗室檢測下限值;或免疫缺陷病毒抗體(HIV-Ab)陽性或梅毒螺旋體抗體(TPAb)呈陽性;
12.(檢查)基線時尿液藥物篩查或酒精呼氣測試結果呈陽性者;
13.(問診)篩選前3個月內男性每周飲酒量大于21 單位,女性大于14單位(1 單位酒精≈360 mL啤酒或45 mL酒精含量為40%的烈酒或150 mL葡萄酒),或試驗期間不能禁酒者;
14. 研究者認為受試者存在任何不宜參加此試驗的其它因素。
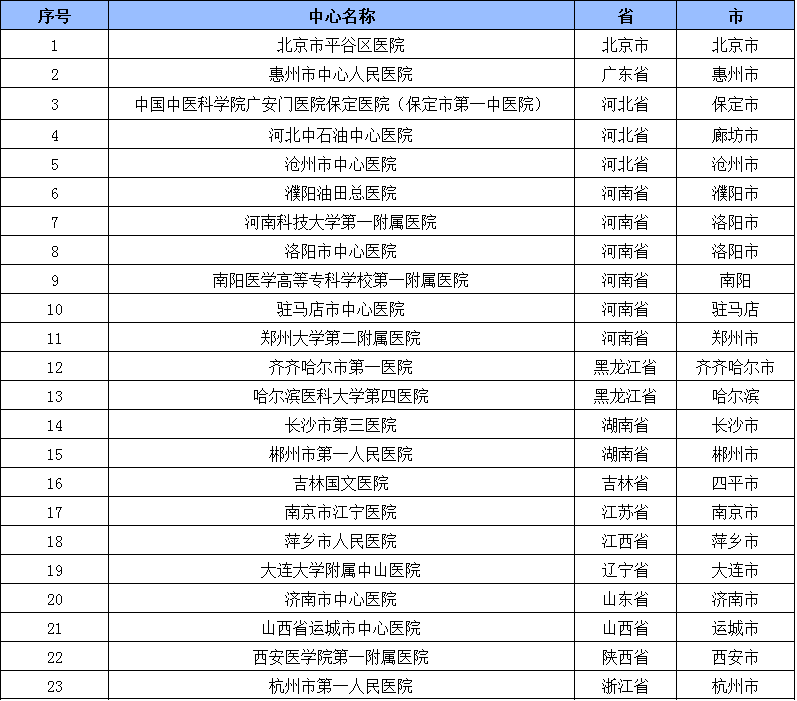
參與機構
試驗信息
試驗分期:Ⅱ期
藥品名稱:MWN101 注射液
適應癥:2型糖尿病
評價MWN101 注射液治療 2 型糖尿病的有效性、安全性及藥代動力學特征的隨機、雙盲、安慰劑及陽性藥平行對照、多中心Ⅱ期臨床研究
主要入選標準
滿足下列所有入選標準才可入選本試驗:
1.(問診)年齡在 18~75 周歲之間(含)且符合《中國 2 型糖尿病防治指南(2020 年版)》診斷標準的中國成人2型糖尿病患者,且滿足以下任意一條標準:
(1) 診斷為2型糖尿病的初治患者,已接受至少8周的飲食和運動干預,且既往未服用過抗糖尿病藥物,或者
(2) 既往診斷的2型糖尿病患者,目前處于飲食和運動干預期,篩選前 8 周內未接受糖尿病藥物治療,經研究者對其病情評價,可以在生活方式干預的基礎上增加試驗藥物治療;
2.(檢查)篩選時體重指數(BMI):23.0kg/㎡≤BMI≤40.0kg/㎡;
3.(檢查)篩選/基線時糖化血紅蛋白(HbA1c)中心實驗室檢測結果滿足:7.0%≤HbA1c≤10.5%;
4.(檢查)篩選/基線時空腹血糖(FPG):FPG≤13.3 mmol/L(如存在影響血糖的特殊因素可在 1 周內復測 1 次);
5.(問診)能夠按照方案要求完成試驗,自愿作為受試者,并簽署知情同意書。
主要排除標準
1.(問診)篩選前12個月內發生過嚴重的糖尿病急性并發癥;
2.(問診及檢查)篩選時存在嚴重的糖尿病慢性并發癥;
3.(問診)篩選前 6 個月內發生過3級低血糖;
4.(問診及檢查)篩選期前6個月發生過以下心血管疾病,如心力衰竭(NYHA 分級為 III-IV 級)、心肌梗塞、冠狀動脈旁路移植術或冠脈支架植入病史、需要治療的嚴重的心律失常,如Ⅱ度或Ⅲ度的房室傳導阻滯、長 QTC 綜合征或 QTc 間期延長(QTcF 女性≥470 ms 或男性≥450 ms);
5.(問診)篩選前 6個月患有出血性或缺血性腦卒中、短暫性腦缺血;
6.(檢查)篩選時甲狀腺功能檢查結果存在具有臨床意義的異常且需要啟動治療;
7.(檢查)篩選時經治療未控制的高血壓(收縮壓≥160 mmHg 和/或舒張壓≥100 mmHg);
8.(問診)既往有急性或慢性胰腺炎病史或臨床證據者;
9.(問診)已知屬于過敏體質(對3種及以上食物或藥物過敏),或對試驗用藥品或其他 GLP-1 受體激動劑類藥物過敏,或篩選時患有嚴重變態反應性疾病(哮喘、蕁麻疹、濕疹性皮炎等);
10.(問診)篩選前采用以下任何一種藥物治療:
(1) 篩選前1年內使用過胰島素,以下情況除外:①使用胰島素治療妊娠糖尿病,②因急性疾病、住院期間或擇期手術等而短期使用(≤2 周)胰島素;
(2) 篩選前 8 周曾使用過其他可能影響血糖代謝的藥物,如其他降糖藥物、全身性糖皮質激素(吸入性或局部外用除外)、生長激素等;
11.(檢查)篩選或基線時實驗室檢查結果符合以下標準的受試者:
(1) 空腹C肽<0.81 ng/mL(0.27 mmol/L);
(2) ALT、AST≥2.5×ULN或血總膽紅素≥1.5×ULN;
(3) 血淀粉酶或血脂肪酶≥1.5×ULN;
(4) 腎小球濾過率(eGFR)<60 mL/min/1.73m2 (CKD-EPI公式)或尿蛋白陽性 2+ 及以上;
(5) 血清降鈣素水平≥35 ng/L(pg/mL);
(6) 甘油三酯≥5.64 mmol/L(500 mg/dL;如為生活方式所致異常,則可在 1 周內復測 1 次);
(7) 血紅蛋白(HGB)<100 g/L;
(8) 乙肝表面抗原(HBsAg)陽性且乙肝病毒載量(HBV-DNA)高于當地實驗室檢測下限值;或丙肝抗體(HCV-Ab)陽性且丙肝病毒載量(HCV-RNA)高于當地實驗室檢測下限值;或免疫缺陷病毒抗體(HIV-Ab)陽性或梅毒螺旋體抗體(TPAb)呈陽性;
12.(檢查)基線時尿液藥物篩查或酒精呼氣測試結果呈陽性者;
13.(問診)篩選前3個月內男性每周飲酒量大于21 單位,女性大于14單位(1 單位酒精≈360 mL啤酒或45 mL酒精含量為40%的烈酒或150 mL葡萄酒),或試驗期間不能禁酒者;
14. 研究者認為受試者存在任何不宜參加此試驗的其它因素。
參與機構
